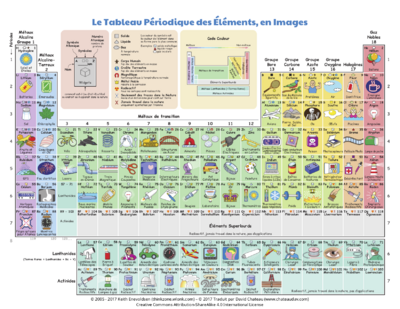
Tableau périodique des éléments
Le tableau périodique des éléments regroupe tous les éléments chimiques connus qui constituent l'Univers : les atomes. Il en manque peut-être dans l'état actuel des connaissances. Ils sont classés en colonnes et en lignes. Dans une même colonne, se trouvent des atomes qui ont des propriétés similaires. Il existe des phrases pour retenir les premières périodes : Hé HÉ (Hydrogène, HÉlium) LIeBE, le Bateau CARéné, Noé et Olivia Filerons Nord - Est (Lithium, Béryllium, CARbone, azote[N], Oxygène, Fluor, Néon). Napoléon Mangea Allègrement Six Poulets Sans Claquer ARGent (sodium [Na], Magnésium, Aluminium, Silicium, Phosphore, Soufre, Chlore, ARGon).
Histoire

Le premier à imaginer une classification des éléments selon leur masse fut le géologue français Alexandre-Émile Béguyer de Chancourtois. Mais son travail ne fut jamais très connu des chimistes car il était géologue et avait employé des mots propres à la géologie dans la publication où il présentait sa classification. Quelques années plus tard le chimiste Dmitri Mendeleïev publia un tableau où il classait les éléments en fonction de leur masse et de leurs propriétés chimiques. Ce tableau était plus complet que celui du géologue français et il permettait de prédire l'existence d'autres éléments là où il y avait des "trous" dans le tableau. Il eu donc beaucoup de succès et même si la classification a beaucoup évolué depuis et que d'autres tableaux ont été proposés, la classification périodique des éléments est encore souvent appelée tableau de Mendeleïev. La classification périodique des éléments fut l'une des plus remarquables avancées de la science moderne.
Construction du tableau
De quoi est constitué un atome ? Il est composé d'un noyau et d'électrons tournant autour de ce noyau. Dans le noyau, se trouvent des protons, qui ont chacun une charge (+) et des neutrons, qui n'ont pas de charge. Chaque électron possède une charge (-). Le nombre d'électrons tournant autour du noyau est égal au nombre de protons. Le nombre de protons est particulier à chaque élément : on en fait donc son numéro atomique, qui est indiqué dans chaque case avec le symbole de l'élément.
La chimie s'occupe uniquement des échanges d'électrons entres atomes, ou molécules, et que le noyau reste inchangé au cours d'une réaction chimique. Il y a donc, dans un atome, autant de charges (+) que de charges (-) : l'atome est neutre, car chaque charge positive est neutralisée par une charge négative. Pour changer la composition du noyau, il faut avoir recours à des réactions nucléaires ou atomiques (nucléaire signifie qui se rapporte au noyau).
Donc la chimie s'intéresse au nombre d'électrons autour d'un atome. Les chimistes ont remarqué que les atomes veulent avoir autour d'eux le même nombre d'électrons que les gaz nobles, aussi appelés gaz rares, de la huitième colonne (hélium, néon, argon, krypton, radon).
La dernière colonne
La dernière colonne est celle des gaz rares. Les chimistes ont observé depuis longtemps que les atomes d'hélium, de néon, d'argon, de krypton et de xénon ne réagissaient chimiquement avec aucun autre composé : ils sont inertes. Mendeleïev les place donc tous dans la dernière colonne de son tableau. En observant la composition électronique de ces atomes, on s'aperçoit qu'ils possèdent tous 8 électrons dans leur périphérie. D'où la règle de l'octet : les atomes ayant 8 électrons en périphérie sont stables. On verra que les autres atomes veulent avoir dans leur couche périphérique 8 électrons pour devenir stables. Ils pourront :
- soit perdre un ou plusieurs électrons, c'est le cas des trois premières colonnes ;
- soit en gagner un ou plusieurs, c'est le cas des deux colonnes précédant celle des gaz rares.
La première et l'avant-dernière colonnes
- La première colonne est celle des métaux alcalins (lithium, sodium, potassium, rubidium, césium). Ils possèdent tous un électron en périphérie. Pour ressembler à un gaz rare et avoir 8 électrons en périphérie, ils doivent simplement perdre un électron. Avant de perdre cette charge -, ils avaient autant de charges + que de charges -. Maintenant, ils ont une charge + en trop. Les métaux de cette colonne vont donc donner des ions avec une charge +, appelés cations.
- L'avant-dernière colonne est celle des halogènes (fluor, chlore, brome, iode). Ils possèdent 7 électrons à leur périphérie. Pour ressembler aux gaz rares qui les suivent et avoir 8 électrons, ils doivent capter un électron. Ils auront alors un électron de plus que de protons. Ils vont donner des ions avec une charge -, appelés anions.
Comme les électrons libres n'existent pas, un donneur d'électron doit rencontrer un accepteur d'électrons. Les éléments de la première colonne peuvent donc rencontrer un élément de l'avant-dernière.
Exemple
Un halogène et un métal alcalin peuvent se lier pour donner un sel. Le sodium et le chlore s'assemblent selon cette règle : le sodium donne un électron au chlore, ce qui fait du chlorure de sodium ou sel de cuisine. Il existe toutes les combinaisons possibles : chlorure de lithium, chlorure de potassium, chlorure de césium, fluorure de lithium, fluorure de potassium, bromure de sodium, bromure de potassium, etc.
| Colonne → | 1 I A |
2 II A |
3 III B |
4 IV B |
5 V B |
6 VI B |
7 VII B |
8 VIII B |
9 VIII B |
10 VIII B |
11 I B |
12 II B |
13 III A |
14 IV A |
15 V A |
16 VI A |
17 VII A |
18 VIII A | |
| ↓ Période | |||||||||||||||||||
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |
| 7 | 87 Fr |
88 Ra |
** |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| * Lanthanides | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | ||||
| ** Actinides | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | ||||
| Métaux alcalins | Métaux alcalino-terreux | Lanthanides | Actinides | Métaux de transition |
| Métaux pauvres | Métalloïdes | Non-métaux | Halogènes | Gaz rares |
Dans des conditions normales de pression et de température :
- Les éléments dont le numéro atomique est rouge sont gazeux ;
- Les éléments dont le numéro atomique est bleu sont liquides ;
- Les éléments dont le numéro atomique est noir sont solides.
(ne pas confondre : la couleur rouge ou bleue du symbole de l'élément indique si Vikidia possède un article sur cet élément)
Dans la nature :
|
|
|
|
Liens externes
|