Azote
| Azote | |
|---|---|
 |
|
| Attributs et classement | |
| Symbole | N |
| Période | 2 |
| Famille | pnictogènes |
| Propriétés physiques | |
| Masse molaire | 14 g/mol |
| État ordinaire | gazeux |
| Température de fusion | -210 ℃ |
| Température d'ébullition | -195 ℃ |
| Masse atomique | 14,0067 u |
| Masse volumique | 1,2506 kg/m3 |
| Autres | |
| Énergie de 1re ionisation | 14,5341 J/mol |
| Valence | 3 |
| Structure électronique | [He] 2s2 2p3 |
| Électronégativité | 3.04 |
| Modifier | voir modèle • modifier |
L'azote est un élément chimique simple de symbole N. On utilise aussi le nom d'azote pour désigner le diazote, qui est un gaz formé par la liaison de deux atomes d'azote entre eux.
Le mot azote signifie sans vie en grec. Antoine Lavoisier l'a appelé ainsi car il s'est rendu compte que des animaux respirant le diazote pur ne pouvaient pas survivre.
L'élément chimique
L'élément azote se définit, comme tous les autres éléments, par la composition de son noyau atomique. Celui-ci contient 7 protons et 7 neutrons. Il existe des atomes d'azote qui possèdent plus de neutrons, ce sont des isotopes de l'azote.
L'azote est situé entre le carbone, qui contient 6 protons, et l'oxygène qui contient 8 protons, dans le tableau périodique des éléments.
Le gaz diazote
Le diazote, appelé couramment azote (comme pour l'oxygène et le dioxygène), est le principal composant gazeux de l'atmosphère. Il compose environ 78% de l'atmosphère.
À la pression de l'atmosphère à la surface de la Terre, l'azote devient liquide à une température de l'ordre de -196 °C. Au-dessus de cette température, c'est un gaz.
Importance de l'azote pour la vie
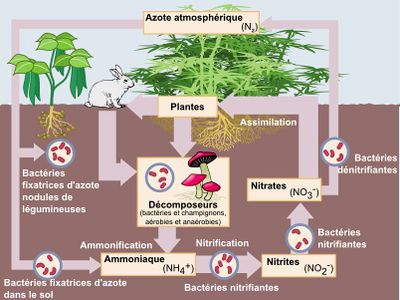
L'azote atmosphérique est utilisable uniquement par des bactéries et champignons vivant dans le sol et au niveau des racines de légumineuses. Les nitrates produits, après plusieurs étapes, sont alors utilisés par les plantes pour fabriquer des protéines, c'est l'assimilation. Ces protéines seront consommées par les herbivores, qui seront à leur tour mangés par les carnivores.
L'élément azote est retrouvé en quantité importante dans les protéines, constituant majeur des protéines et des êtres vivants. C'est d'ailleurs la seule source d'azote que l'homme et les animaux peuvent utiliser : c'est pour cette raison qu'il faut manger des aliments contenant des protéines. Ce sont celles-ci qui fourniront l'azote dont on a besoin. Les plantes peuvent utiliser quant à elles des nitrates. L'homme peut donc donner de l'engrais dit azoté aux plantes qu'il cultive pour augmenter le rendement agricole.
Dans la nature, seuls quelques organismes sont capables d'utiliser l'azote de l'air. Ce sont des bactéries ou des champignons unicellulaires et microscopiques qui vivent dans les racines de certaines plantes et forment une symbiose avec la plante. Ces plantes sont par exemple les légumineuses, comme la luzerne ou le trèfle. Ces micro-organismes fixateurs d'azote sont extrêmement importants dans le cycle de l'azote, et donc dans la vie.
Importance de l'azote dans l'industrie
L'azote est retrouvé dans des composés chimiques importants pour l'industrie : les nitrates sont importants pour produire par exemple des engrais utilisés dans l'agriculture, l'ammoniac est utilisé dans énormément d'applications, comme par exemple la fabrication d'explosif (comme la poudre de salpêtre) ou bien la confection de plastiques. Le gaz azote est aussi très utilisé car il est facile à produire et permet d'obtenir des températures très basses, pour conserver des cellules dans les laboratoires de recherche par exemple, etc.
Pourquoi le symbole N ?
L'azote est désigné dans la nomenclature chimique par la lettre N et non par la lettre A. Pourquoi ?
Tout simplement parce que le symbole des atomes est un symbole international, et pas en français. En latin, « azote » se dit Nitrogenium, et en anglais, Nitrogen, d'où le 'N'. On le retrouve d'ailleurs dans les divers composés de l'azote : le Nitre, ou nitrate de potassium, également appelé salpêtre.
Cela aurait pu toutefois se faire car le terme est formé sur du grec (qui veut dire littéralement "sans vie") : il a existé à une époque un symbole Az pour l'azote (avant l'adoption d'un système international), mais il n'a pas été retenu.
Sources
- Azote - Diazote - Fixation biologique de l'azote. Wikipédia. Consultés le 5 octobre 2007.
| Colonne → | 1 I A |
2 II A |
3 III B |
4 IV B |
5 V B |
6 VI B |
7 VII B |
8 VIII B |
9 VIII B |
10 VIII B |
11 I B |
12 II B |
13 III A |
14 IV A |
15 V A |
16 VI A |
17 VII A |
18 VIII A | |
| ↓ Période | |||||||||||||||||||
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |
| 7 | 87 Fr |
88 Ra |
** |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| * Lanthanides | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | ||||
| ** Actinides | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | ||||
| Métaux alcalins | Métaux alcalino-terreux | Lanthanides | Actinides | Métaux de transition |
| Métaux pauvres | Métalloïdes | Non-métaux | Halogènes | Gaz rares |
|